Elenco di elementi
»
afnio
»
americio
»
Argento
»
argo
»
arsenico
»
astato
»
attinio
»
azoto
»
bario
»
berillio
»
bismuto
»
bohrium
»
Boro
»
bromo
»
cadmio
»
calcio
»
carbonio
»
cerio
»
cesio
»
cloro
»
cobalto
»
cromo
»
curio
»
dubnio
»
elio
»
erbio
»
europio
»
fermium
»
ferro
»
flerovio
»
fluoro
»
fosforo
»
francium
»
gallio
»
germanio
»
hassium
»
idrogeno
»
indio
»
iodio
»
iridio
»
itterbio
»
ittrio
»
krypton
»
lantanio
»
latta
»
litio
»
lutezio
»
magnesio
»
mercurio
»
neodimio
»
neon
»
nettunio
»
nichel
»
Nihonium
»
niobio
»
Nobelium
»
olmio
»
oro
»
osmio
»
ossigeno
»
palladio
»
platino
»
plutonio
»
polonio
»
portare
»
potassio
»
prometeo
»
radio
»
radon
»
rame
»
renio
»
rodio
»
rubidio
»
rutenio
»
samario
»
scandio
»
selenio
»
silicio
»
sodio
»
stronzio
»
tallio
»
tantalio
»
tecnezio
»
tellurio
»
Tennesse
»
terbio
»
titanio
»
torio
»
tulio
»
uranio
»
vanadio
»
xeno
»
zinco
»
zirconio
»
zolfo
Ar - argo - NESSUN GAS METALLO NOBILE
L'argon è un elemento chimico della famiglia dei gas nobili, simbolo Ar e numero atomico 18. Viene prodotto dalla separazione frazionata dei gas presenti nell'aria, principalmente da ossigeno e azoto. È inodore, incolore e inerte.
L'argon è un gas inerte allo stato gassoso, che forma molecole di otto atomi (Argon Atoms – Ar8). La sua massa molare è 39,948 g/mol. Le sue caratteristiche lo rendono molto stabile in ambienti asettici. È il terzo gas nobile più abbondante nell'atmosfera, costituendo lo 0,94% dell'aria. La sua temperatura di ebollizione e la tensione di vapore saturano rispettivamente a -186°C e 0,52 MPa.
L'argon è un cattivo conduttore termico ed elettrico, quindi viene utilizzato per la saldatura e il riempimento di prodotti elettronici e per il riempimento di lampade fluorescenti. Viene anche utilizzato come gas di protezione, poiché non è combustibile e non reagisce con altre molecole.
L'argon è utilizzato in molte applicazioni, inclusa la metallurgia, per riempire gli incendi, per la produzione di prodotti chimici e isolanti, per il riempimento di lampade fluorescenti e per l'inertizzazione di recipienti pressurizzati e involucri dove vengono utilizzate alte temperature. L'argon è anche utilizzato nell'analisi gascromatografica per separare le miscele e misurare la concentrazione dei singoli gas. Infine, l'argon viene utilizzato per la produzione di farmaci, ad esempio l'antidolorifico lidocaina.
L'argon è un gas inerte allo stato gassoso, che forma molecole di otto atomi (Argon Atoms – Ar8). La sua massa molare è 39,948 g/mol. Le sue caratteristiche lo rendono molto stabile in ambienti asettici. È il terzo gas nobile più abbondante nell'atmosfera, costituendo lo 0,94% dell'aria. La sua temperatura di ebollizione e la tensione di vapore saturano rispettivamente a -186°C e 0,52 MPa.
L'argon è un cattivo conduttore termico ed elettrico, quindi viene utilizzato per la saldatura e il riempimento di prodotti elettronici e per il riempimento di lampade fluorescenti. Viene anche utilizzato come gas di protezione, poiché non è combustibile e non reagisce con altre molecole.
L'argon è utilizzato in molte applicazioni, inclusa la metallurgia, per riempire gli incendi, per la produzione di prodotti chimici e isolanti, per il riempimento di lampade fluorescenti e per l'inertizzazione di recipienti pressurizzati e involucri dove vengono utilizzate alte temperature. L'argon è anche utilizzato nell'analisi gascromatografica per separare le miscele e misurare la concentrazione dei singoli gas. Infine, l'argon viene utilizzato per la produzione di farmaci, ad esempio l'antidolorifico lidocaina.
sintetico
Radioattivo
Liquido
Gassoso
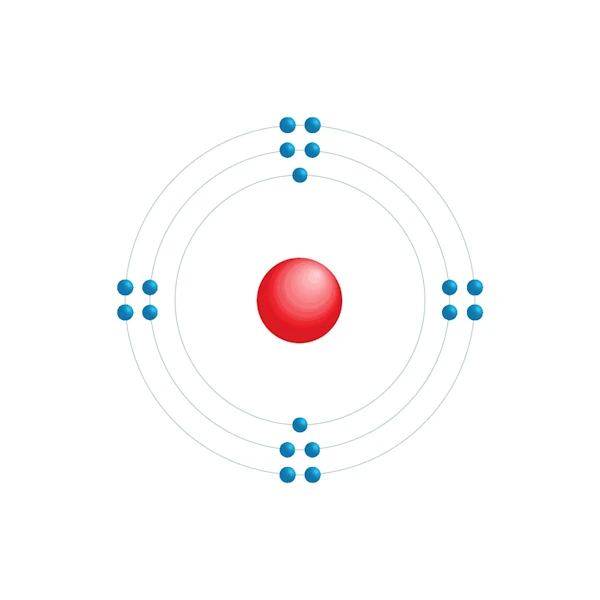
Schema di configurazione elettronico
| Nome | argo |
| Numero | 18 |
| Atomico | 39.948 |
| Simbolo | Ar |
| Fusione | -189.4 |
| Bollente | -185.9 |
| Densità | 0.0017837 |
| Periodo | 3 |
| Gruppo | 18 |
| Scoperta | 1894 Rayleigh and Ramsay |
| Abbondanza | 3.5 |
| Raggio | 0.88 |
| Elettronegatività | 0 |
| Ionizzazione | 15.7596 |
| Numero di isotopi | 8 |
| Configurazione elettronica | [Ne] 3s2 3p6 |
| Stati di ossidazione | 0 |
| Elettrone per livello di energia | 2,8,8 |
 mineraly.fr
mineraly.fr
 mineraly.co.uk
mineraly.co.uk
 mineraly.com.de
mineraly.com.de
 mineraly.it
mineraly.it
 mineraly.es
mineraly.es
 mineraly.nl
mineraly.nl
 mineraly.pt
mineraly.pt
 mineraly.se
mineraly.se